Neste material você vai ter acesso a informações sobre o patógeno causador da mancha zonada do arroz, tais como:
- Descrição dos sintomas;
- Identificação do agente causal;
- Epidemiologia;
- Histórico e importância da doença.
A ocorrência de pragas e doenças na lavora orizícola vem ganhando importância nos últimos anos. Se pensarmos na produção de arroz há 12 anos, o manejo de doenças era considerado secundário.
Com o aumento na produtividade de grãos, a proteção da lavoura ganhou importância. Vários pesquisadores destacam que, a ocorrência de epidemias, bem como o surgimento e a agressividade das doenças, está diretamente relacionado com o tipo de cultivar utilizada, densidade de semeadura e práticas de manejo de maneira geral.
Nesse sentido, é importante dar atenção àquelas doenças que geralmente causam danos em todos os anos, caso da Brusone (Pyricularia grisea), Mancha parda (Bipolaris oryzae), queima das bainhas (Rhizoctonia solani) e escaldadura das folhas (Gerlachia oryzae), assim como, monitorar aquelas com importância secundária.
Diversas plantas de arroz irrigado foram trazidas ao laboratório de microbiologia do Instituto Phytus para identificação de doença. Técnicos e produtores estavam preocupados com uma mancha atípica que estava atacando a cultura já na fase de plântula e perfilhamento.
Descrição dos sintomas
As lesões da doença normalmente eram pequenas manchas ovais ou circulares de cor marrom ou pardas com centro acinzentado e contorno marrom avermelhadas (Figura 1). Em algumas lesões foram observadas estruturas globosas de coloração escura, possivelmente peritécios (Figura 2).
Quando em estágio mais avançado, estas manchas coalescem, formando “zonas” nas folhas (Figura 3), comprometendo dessa forma a área fotossinteticamente ativa. O início da doença pode ser facilmente confundido com a mancha circular (Alternaria padwickii) e a Brusone (Pyricularia grisea).



Identificação do agente causal
Inicialmente foram utilizadas duas metodologias para identificação do patógeno:
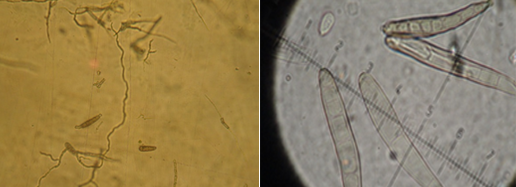
1ª – Isolamento em meio de cultura Batata-dextrose-ágar (BDA) com incubação a 22°C e fotoperíodo de 12 horas por 5 dias e, câmara úmida utilizando folhas com sintomas, nas mesmas condições já citadas. No quarto dia de incubação foi possível perceber estruturas escuras arredondadas no centro das manhas, assemelhando-se a um peritécio (FIGURA 2). Ao examinar a estrutura com auxílio de um microscópio ótico, constatou-se que se tratava da fase teleomórfica (sexual) de um fungo.
Baseado nas características dos ascósporos, bem como dos sintomas, excluiu-se a possibilidade da doença estar sendo causada por Bipolaris oryzae, Drechslera oryzae ou Alternaria padwickii. Após consulta na literatura, concluiu-se que se tratava provavelmente da fase sexual de Drechslera gigantea (Pyrenophora gigantea)(FIGURA 4). Após realizar o isolamento de diversas amostras de arroz, desde o perfilhamento até planta adulta, verificou-se que, dependendo da cultivar e do local, era possível identicar tanto a fase teleomórfica, quanto a fase anamórfica (Drechslera gigantea syn. Helminthosporium giganteum) do fungo (FIGURA 5), não havendo, porém, uma tendência para ocorrência de um ou outro.
2ª – Para confirmação do agente causal foi realizado o Postulado de Koch, procedimento que auxilia na identificação a partir da patogenicidade do fungo sobre um hospedeiro suscetível. O postulado basicamente consiste em promover condições de crescimento do organismo associado aos sintomas e, posteriormente manter a cultura pura do organismo em meio artificial.
– Isolamento
Para o isolamento foram selecionadas as áreas de transição entre o tecido infectado e o tecido sadio das folhas de onde foram retirados fragmentos com auxílio de um bisturi. Posteriormente, estes fragmentos foram submetidos à desinfecção superficial, sendo imersos em álcool 70%, hipoclorito de sódio 1% e três lavagens em água destilada estéril, por um minuto em cada solução. Após, os fragmentos foram postos sobre papel filtro estéril na câmara de fluxo laminar, por aproximadamente 10 minutos para secagem. Finalmente os fragmentos foram depositados em placas de petri contendo meio de cultura BDA e incubados em temperatura de 23 °C e fotoperíodo de 12 horas, por aproximadamente 5 dias.
Após este período, as estruturas foram observadas em lupa e microscópio optico para identificação do patógeno. O reisolamento dos sintomas observados nas plantas inoculadas (Figura 7), confirmou o agente causal como sendo Drechslera gigantea. O fungo apresentava conidióforo marrom com 1 a 7 septos, conídios medindo 166- 485 x 10-29 ?m, sendo que, a germinação do esporo ocorre ou na base ou no ápice do esporo, mas raramente no meio. Em meio de cultura V8, a cultura apresentava aspecto cotonoso de coloração cinza-escura a olivácea, de acordo com o que está descrito na literatura (Shoemaker, 1959; Ahn, 1980).


Epidemiologia
Pelo fato de ter sido identificada em plântulas de arroz, é provável que, haja transmissão via sementes da doença. A germinação de conídios do patógeno ocorre entre 15 e 23 °C, sendo que, quanto maior o período de orvalho, maior será a severidade da doença (GREEN et al., 2004).
Histórico e importância da doença
A primeira ocorrência da doença na sua fase anamórfica se deu em 1979 em arroz selvagem na Colômbia, Panamá e Peru (Ahn, 1980). Posteriormente, a doença foi identificada causando danos em campos experimentais de arroz selvagem da Universidade de Minessota (USA). Na safra 2003, D. gigantea foi identificada em plantas de trigo, provocando inúmeras lesões circulares e ovais com margem marrom e centro cinza (CHOWDHURY et al, 2005). Em plantas de arroz cultivado, foi identificado na Venezuela (RODRIGUEZ & NASS, 1990).
Na safra de 2006/2007 o patógeno foi identificado causando manchas nas cultivares BRS Querência e BRS Atalanta em lavouras de Capão do Leão/RS, sendo que, na safra seguinte a doença demonstrou alta severidade nos estádios finais do desenvolvimento de arroz no mesmo local (NUNES, 2008).
O patógeno provoca mancha zonada em bananeira e espécies de gramas, sendo também utilizado como agente bioherbicida no controle de Setaria viridis da família Poaceae, erva daninha comum no Canadá, resistente aos herbicidas inibidores da Acetyl-CoA Carboxylase e Digitaria sanguinalis na Florida. Drechslera gigantea pode provocar mancha zonada em: Agropyron, Agrostis, Anthephora, Bambusa, Bromus, Cenchrus, Commelina, Cynodon, Dendrocalamus, Echinochloa, Eleusine,Elymus, Eragrostis, Festuca, Glyceria, Hilaria, Lasiagrostis, Leersia, Melinis, Musa, Oryza, Panicum, Pennisetum, Phalaris, Poa, Saccharum, Sporobolus, Teramnus, Trichachne, Uniola, Zinnia (SIVANESAN, 1992).
Tendo em vista a grande incidência dessa doença nas safras 2014 e 2015 e também considerando o grande número de hospedeiros alternativos de Drechslera gigantea, é de grande importância conhecer melhor esse patossistema, bem como, estudar o seu comportamento frente a práticas culturais que possam interferir no ciclo da doença. Além disso, é necessário investigar a respeito do controle químico, tanto via tratamento de sementes, quanto, em parte aérea, bem como conhecer o nível de sensibilidade à doença das principais cultivares utilizadas no estado.
Apesar de não se ter ainda conhecimento sobre nível de danos econômicos causados pela doença, a sua ocorrência e severidade nas últimas duas safras demonstra que devemos dar mais atenção, evitando surpresas no futuro.
Referências
CABI. 2015. Crop Protection Compendium. Drechslera gigantea. Obtido na Internet: http://www.cabicompendium.org/cpc/datasheet.asp, em 13/01/2015.
CHOWDHURY, A-K; GARAIN, P-K; MUKHERJEE, S; DUTTA, S; BHATTACHARYA, P. M; SINGH, D. P; GYANENDRA,S. Zonate eyespot of wheat – a new report. Journal of Mycopathological Research, Calcutta, v. 43, n. 1, p. 139-140, 2005.
EVIDENTE, A.; ANDOLFI, A.; CIMMINO, A.; VURRO, M.; FRACCHIOLLA, M.; CHARUDATTAN, R. Herbicidal potential of ophiobolins produced by Drechslera gigantea. Journal of Agricultural and Food Chemistry. v.54, n.5, p.1779-1783, 2006.
GREEN, S.; PENG, G.; CONNOLLY, T.; BOYETCHKO, S. M. Effect of moisture and temperature on disease of green foxtail caused by Drechslera gigantea and Pyricularia setariae. Plant Disease, St. Paul, v. 88, n. 6, p. 605-612, 2004.
SIVANESAN, A. Drechslera gigantea. (Descriptions of fung and bacteria). Wallingford: CAB International, 1992. p.113.
WEIKERT-OLIVEIRA, R. A. C. B.; RESENDE, M. A.; VALÉRIO, H. M.; CALIGIORNE, R. B.; PAIVA, E. Genetic variation among pathogens causing “helminthosporium” diseases of rice, maize and wheat. Fitopatologia Brasileira, Brasília, DF, v. 27, n. 6, p. 639-643, 2002




