O material didático traz informações sobre os fungicidas protetores orgânicos e suas principais classes:compostos aromáticos, ditiocarbamatos, organoestânicos e guanidinas.
Neste material você vai encontrar uma breve descrição dos principais subgrupos dentro dos fungicidas protetores orgânicos.
Os fungicidas protetores orgânicos sofrem alteração/degradação após entrar em contato com luz, água e oxigênio.
Eles são subdivididos em 4 principais grupos baseados em suas características químicas e estruturais:
- Compostos aromáticos
- Organoestânicos
- Ditiocarbamatos
- Guanidina
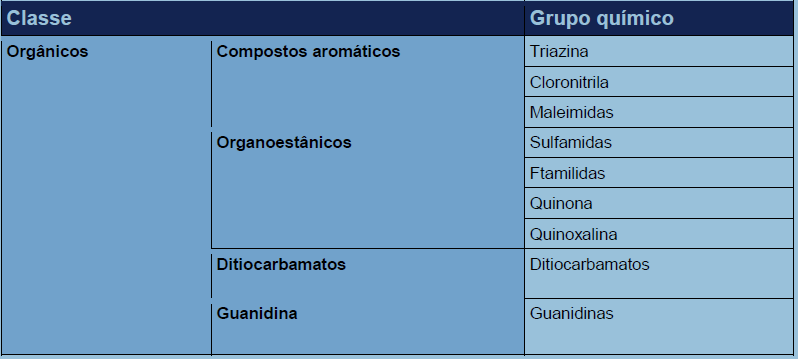
Quadro 1 – Fungicidas protetores orgânicos e inorgânicos e respectivos grupos químicos (Adaptado de: FRAC, 2017; RODRIGUES, 2006).
Compostos Aromáticos: Clorotalonil
Os fungicidas orgânicos da classe dos compostos aromáticos são assim chamados, pois apresentam um ou mais anéis benzênicos em sua molécula.
O anel benzênico (ou anel aromático), representado pela fórmula C6H6, é uma estrutura cíclica muito estável, que se caracteriza pela alternância de ligações simples e duplas entre os carbonos.
O clorotalonil é um exemplar do grupo das cloronitrilas. É um fungicida de amplo espectro que apresenta controle sobre doenças do Grupo I (podridões em órgãos de armazenamento) e Grupo V (manchas foliares, ferrugem, oídio e míldio) de acordo com a classificação de McNew (1960).
Mecanismo de ação do clorotalonil
<
Seu principal mecanismo de ação envolve reações com grupos sulfidrilas e glutationas presentes em proteínas e cofatores de fungos (Roberts et al., 1999).
Estas enzimas são chave em diversos processos fisiológicos importantes no metabolismo celular, sem as quais a formação do ATP é inibida.
O clorotalonil afeta a respiração celular do patógeno, prendendo a glutationa presente no interior da célula.
Várias enzimas envolvidas na respiração celular dependem da glutationa para poder funcionar, por conseguinte, quando o Clorotalonil liga-se a essa proteína, ele interrompe a respiração celular do fungo, o que interrompe o fornecimento de energia e, portanto, impede o desenvolvimento do patógeno.
O retardamento do crescimento micelial do fungo e a inibição da germinação dos esporos são os sintomas da interação entre Clorotalonil e células fúngicas.
Fungicidas Organoestânicos
São substâncias fungicidas que contêm átomos de estanho (Sn) caracterizados principalmente por hidróxido de fentina, acetato de fentina e cloreto de fentina.
São fungicidas não-sistêmicos com ação protetora apresentando alguma ação curativa.
São utilizados no controle de doenças em diversas culturas e no controle de algas e lesmas em campos de arroz. Seu uso em casa de vegetação pode provocar injúrias.
Previnem a germinação de esporos e inibem o metabolismo de fungos, particularmente a respiração, inibem a fosforilação oxidativa na mitocôndria e induzem a peroxidação de lipídios.
Baixas concentrações de compostos organoestânicos inibem a translocação de H+ ligados a membrana, de H+ ATPase e de íons como Na+ e K+(Papa et al., 1982; Powers & Beavis, 1991).
Pela classificação do FRAC (Comitê de Ação à Resistência de Fungicidas) estes compostos atuam como inibidores da fosforilação oxidativa, na ATP-sintase (FRAC, 2016).
Fungicidas Ditiocarbamatos
São compostos derivados do ácido ditiocarbâmico. São caracterizados por monoaminas secundárias que reagem com dissulfeto de carbono, obtendo-se dialquil ditiocarbamatos: dimetil-ditiocarbamatos (DMDC), etileno-bisditiocarbamatos (EBDCs), mono-metildimetilcarbamato e propilenobis-ditiocarbamato
Ditiocarbamatos que possuem grupos hidrofílicos, tais como OH- e COOH, formam complexos de metais pesados solúveis em água.
Entretanto, complexos de metal de ditiocarbamato usados como fungicidas são todos insolúveis em água, mas solúvel em solventes não-polares
- No ano de 1934, surgiu o primeiro fungicida da classe dos ditiocarbamatos Tiram (para patógenos de solo e sementes), seguido de Ferbam (1942) e Ziram (1944).
Estes compostos tinham menor potencial fitotóxico para as plantas, comparados aos compostos à base de cobre ou enxofre, os que também eram utilizados em pulverizações.
Dentro do grupo dos fungicidas protetores orgânicos ditiocarbamatos, temos o subgrupo dos etileno-bisditiocarbamatos (EBDC´s), que são sais orgânicos de manganês, zinco ou zinco e sódio, insolúveis em água e em solventes orgânicos.
São instáveis em meio alcalino ou ácido, na presença de oxigênio, bem como em sistemas biológicos, decompõem-se rapidamente em água.
São produzidos pela reação de dissulfeto de carbono (CS2) com uma amina em condições alcalinas, podendo ocorrer precipitação com sal de metal pesado de natureza polimérica e definição incompleta, especialmente na presença de alguns íons metálicos.
- O primeiro EBDC foi Nabam (1943), seguido de Zinebe (1944), Manebe (1950).
- Foi só no ano de 1962 que pesquisadores registraram Mancozebe (um complexo de íons de zinco com manebe), o que deu origem ao mais importante e significante em termos de comercialização entre todos os EBDCs.

Guanidina
Sabe-se que este subgrupo, que tem nomes comuns Dodina, Guazatine e Iminoctadine, possui atividade protetora multissítio de contato, com alguma ação curativa, porém, ainda não tem modo de ação conhecido (FRAC, 2014).
O Comitê de Ação à Resistência de fungicidas (FRAC) propôs uma ação que afeta as funções da membrana celular e a biossíntese de lipídios em diferentes sítios dos inibidores da demetilação de esteróis.
O mecanismo de ação primária seria afetando a estrutura da membrana da célula através de atividade detergente e da mudança de permeabilidade. Este mecanismo também está relacionado com a membrana mitocondrial.
Enquanto a cadeia lipofílica do fungicida é dissolvida na seção lipídica da membrana, resíduos de guanidina permanecem na fase aquosa e interagem com os fosfolipídios dos grupamentos fosfatos. Dodina afeta a membrana externa de alguns esporos de fungos. Trabalhos com mitocôndrias de ratos indicaram que a guanidina afeta a fosforilação oxidativa (Delen & Tosun, 2003; Tomlin, 2002).
O fungicida apresenta controle doenças dos Grupos V (manchas foliares). Sabe-se que existe caso de resistência conhecida à Venturia inaequalis, nome comum sarna da maçã, (FRAC), tendo um risco baixo a médio ao aparecimento de organismos resistentes.
Com relação à fitotoxicidade do fungicida nas plantas, espécies Frutíferas como, pêssego, ameixa, videira e framboesa podem sofrer injúrias, além disso, pode ocorrer russeting em algumas cultivares de maçã, incluindo Golden Delicous (Tomlin, 1997;Tomlin, 2002).


REFERÊNCIAS BIBLIOGRÁFICAS
DELEN, N.; TOSUN, N. Fungicidas: mecanismo de ação e resistência. Parte 1: fungicidas com mecanismo de ação não-específica. In: Luz, W.C.; Fernandes, J.M.; Prestes, A.M.; Picinini, E.C. Revisão anual de patologia de plantas. v.11, 2003. p.43-69.
FISHEL, F, M. Fungicide Resistance Action Committee’s (FRAC) Classification Scheme of Fungicides According to Mode of Action. University of Florida, IFAS Extension, PL 94, 9p.
FRAC. Fungicide Resistance Action Committee (FRAC): http://www.frac.info/
GARCIA, A. Fungicidas I: utilização no controle químico de doenças e sua ação contra os fitopatógenos. Porto Velho: EMBRAPA-CPAF Rondônia, 1999. 32p. (EMBRAPA-CPAF Rondônia. Documentos, 46).
GULLINO, M. L. et al. Mancozeb: Past, present and future, Plant Disease, v. 94, n. 9, p. 1076-1087, 2010.
RODRIGUES, M. A. T. Classificação de fungicidas de acordo com o mecanismo de ação proposto pelo FRAC. Dissertação apresentada à Faculdade de Ciências Agronômicas da UNESP- Campus de Botucatu, para obtenção do titulo de Mestre em Agronomia, 2006. 249p.
TOMLIN, C. D. S. The pesticide manual – a world compendium. Surrey, UK: British Crop Protection Council. 11 ed., 1997. p. 1252-4.
TOMLIN, C.D.S. The pesticide manual: a world compendium. Surrey, Uk: British Crop Protection Council, 12 ed., 2002.1 – CD-ROM.





2 respostas
Qual o nome dos produtos orgânicos mencionados na reportagem
Olá Regina, tudo bem?
Os fungicidas protetores orgânicos citados no conteúdo podem ser encontrados no mercado com diversos nomes comerciais. Você pode encontrar a listagem completa no site AGROFIT, do Ministério da Agricultura, Pecuária e Abastecimento, pesquisando pelos grupos químicos na aba Ingredientes Ativos cons.
Espero ter ajudado!
Abraços!